Solubility é a capacidade de um soluto de se dissolver em um solvente . A solubilidade de uma substância em outra não é ilimitada, e a quantidade de soluto que você pode resolver em um solvente varia muito. Os valores tabulados de solubilidade referem-se a gramas máximas de soluto em uma determinada quantidade do solvente.
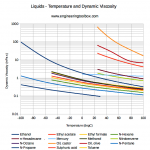
- solubilidade depende da temperatura. Em geral, mas não sem expectativas, a solubilidade aumenta com a temperatura
- smaller particles dissolve faster than larger particles
- a solid dissolves more quickly if the mixture is shaken or shaken
An saturated solution contém a quantidade máxima de soluto no solvente, dada pela solubilidade.
Exemplos de soluções comuns:
- chá com açúcar – uma solução de açúcar em água quente (chá)
- água do mar – uma solução de sal em água
Exemplo 1
Sodium chloride, NaCl, is the salt used for cooking. This salt has a solubility of 36 g in 100 g of water at 25°C.
What is the concentration (by weight%) of a saturated aqueous NaCl solution at 25°C?
A saturated solution contains the maximum amount of solute in the solvent, which for NaCl is 36 grams in water at 25°C. So, the concentration of the saturated solution is: g NaCl /g NaCl solution *100%
NaCl concentration = 36 [g]/(100 + 36)[g] * 100% = 26.5% by weight
Example 2
What will be the concentration (by weight%) if you add 34 g of NaCl to 100 g of water?
34 g of NaCl is less than the solubility, which means that all of the salt will dissolve in water at 25°C.
NaCl concentration = 34 [g]/(100+34) [g] * 100% = 25.4% by weight
Example 3
What will the concentration (by weight%) of the saline solution be if you add 38 g of NaCl to 100 g of water?
38 g of NaCl is more than the solubility of NaCl in water. This means that the solution will become saturated and part of the salt will remain undissolved at 25°C. The concentration of the saturated solution is the same as in Example 1:
NaCl concentration = 36 [g]/(100 + 36)[g] * 100% = 26.5% by weight
Source: https://www.engineeringtoolbox.com/solubility-d_1283.html