Solubilidad es la capacidad de un soluto para disolverse en un solvente. La solubilidad de una sustancia en otra no es ilimitada y la cantidad de soluto que puede disolver en un solvente varía mucho. Los valores de solubilidad tabulados se refieren a gramos máximos de soluto en una cantidad dada de solvente.
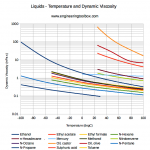
- la solubilidad depende de la temperatura. En general, pero no sin expectativas, la solubilidad aumenta con la temperatura.
- las partículas más pequeñas se disuelven más rápido que las partículas más grandes
- un sólido se disuelve más rápidamente si la mezcla se agita o agita
Un solución saturada contiene la cantidad máxima de soluto en el solvente, dada por la solubilidad.
Ejemplos de soluciones comunes:
- té con azúcar – una solución de azúcar en agua caliente (té)
- agua de mar – una solución de sal en agua
Ejemplo 1
El cloruro de sodio, NaCl, es la sal que se usa para cocinar. Esta sal tiene una solubilidad de 36 g en 100 g de agua a 25°C.
¿Cuál es la concentración (en peso%) de una solución acuosa saturada de NaCl a 25°C?
Una solución saturada contiene la máxima cantidad de soluto en el solvente, que para NaCl es de 36 gramos en agua a 25°C. Entonces, la concentración de la solución saturada es: g NaCl /g solución NaCl * 100%
concentración de NaCl = 36 [g]/(100 + 36) [g] * 100% = 26,5% en peso
Ejemplo 2
¿Cuál será la concentración (% en peso) si agrega 34 g de NaCl a 100 g de agua?
34 g de NaCl es menos que la solubilidad, lo que significa que toda la sal se disolverá en agua a 25°C.
concentración de NaCl = 34 [g]/(100+34) [g] * 100% = 25,4% en peso
Ejemplo 3
¿Cuál será la concentración (en peso%) de la solución salina si agrega 38 g de NaCl a 100 g de agua?
38 g de NaCl es más que la solubilidad de NaCl en agua. Esto significa que la solución se saturará y parte de la sal permanecerá sin disolver a 25°C. La concentración de la solución saturada es la misma que en el Ejemplo 1:
concentración de NaCl = 36 [g]/(100 + 36) [g] * 100% = 26,5% en peso
Fuente: https://www.engineeringtoolbox.com/solubility-d_1283.html