Solubilidade é a capacidade de um soluto de se dissolver em um solvente . A solubilidade de uma substância em outra não é ilimitada, e a quantidade de soluto que você pode resolver em um solvente varia muito. Os valores tabulados de solubilidade referem-se a gramas máximas de soluto em uma determinada quantidade do solvente.
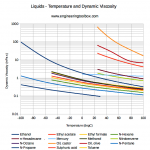
- solubilidade depende da temperatura. Em geral, mas não sem expectativas, a solubilidade aumenta com a temperatura
- partículas menores se dissolvem mais rápido do que partículas maiores
- um sólido se dissolve mais rapidamente se a mistura for agitada ou agitada
Uma solução saturada contém a quantidade máxima de soluto no solvente, dada pela solubilidade.
Exemplos de soluções comuns:
- chá com açúcar – uma solução de açúcar em água quente (chá)
- água do mar – uma solução de sal em água
Exemplo 1
O cloreto de sódio, NaCl, é o sal usado para cozinhar. Este sal tem uma solubilidade de 36 g em 100 g de água a 25°C.
Qual é a concentração (em peso%) de uma solução aquosa saturada de NaCl a 25°C?
Uma solução saturada contém a quantidade máxima de soluto no solvente, que para NaCl é 36 gramas em água a 25°C. Então, a concentração da solução saturada é: g NaCl /g NaCl solução *100%
Concentração de NaCl = 36 [g]/(100 + 36)[g] * 100% = 26,5% em peso
Exemplo 2
Qual será a concentração (em peso%) se você adicionar 34 g de NaCl a 100 g de água?
34 g de NaCl é menor que a solubilidade, o que significa que todo o sal será dissolvido em água a 25°C.
Concentração de NaCl = 34 [g]/(100+34) [g] * 100% = 25,4% em peso
Exemplo 3
Qual será a concentração (em peso%) da solução salina se você adicionar 38 g de NaCl a 100 g de água?
38 g de NaCl é mais do que a solubilidade do NaCl em água. Isso significa que a solução ficará saturada e parte do sal permanecerá não dissolvido a 25°C. A concentração da solução saturada é a mesma do Exemplo 1:
Concentração de NaCl = 36 [g]/(100 + 36)[g] * 100% = 26,5% em peso
Fonte: https://www.engineeringtoolbox.com/solubility-d_1283.html